Július 5-én a Novo Nordisk elindította Kínában a CagriSema injekció III. fázisú klinikai vizsgálatát, amelynek célja a CagriSema injekció és a szemeglutid biztonságosságának és hatékonyságának összehasonlítása Kínában elhízott és túlsúlyos betegeknél.
A CagriSema injekció a Novo Nordisk fejlesztése alatt álló, hosszú hatású kombinált terápia, melynek fő összetevői a GLP-1 (glükagonszerű peptid-1) receptor agonista smeglutid és egy hosszú hatású amilin analóg cagrilintide.A CagriSema injekciót hetente egyszer lehet beadni szubkután.
Az elsődleges cél a CagriSema (2,4 mg/2,4 mg) összehasonlítása szemeglutiddal vagy placebóval hetente egyszer, szubkután.A Novo Nordisk bejelentette a CagriSema 2-es stádiumú cukorbetegség kezelésére szolgáló kísérletének eredményeit, amely bebizonyította, hogy a CagriSema hipoglikémiás hatása jobb, mint a szemeglutidé, és az alanyok közel 90%-a elérte a HbA1c célt.
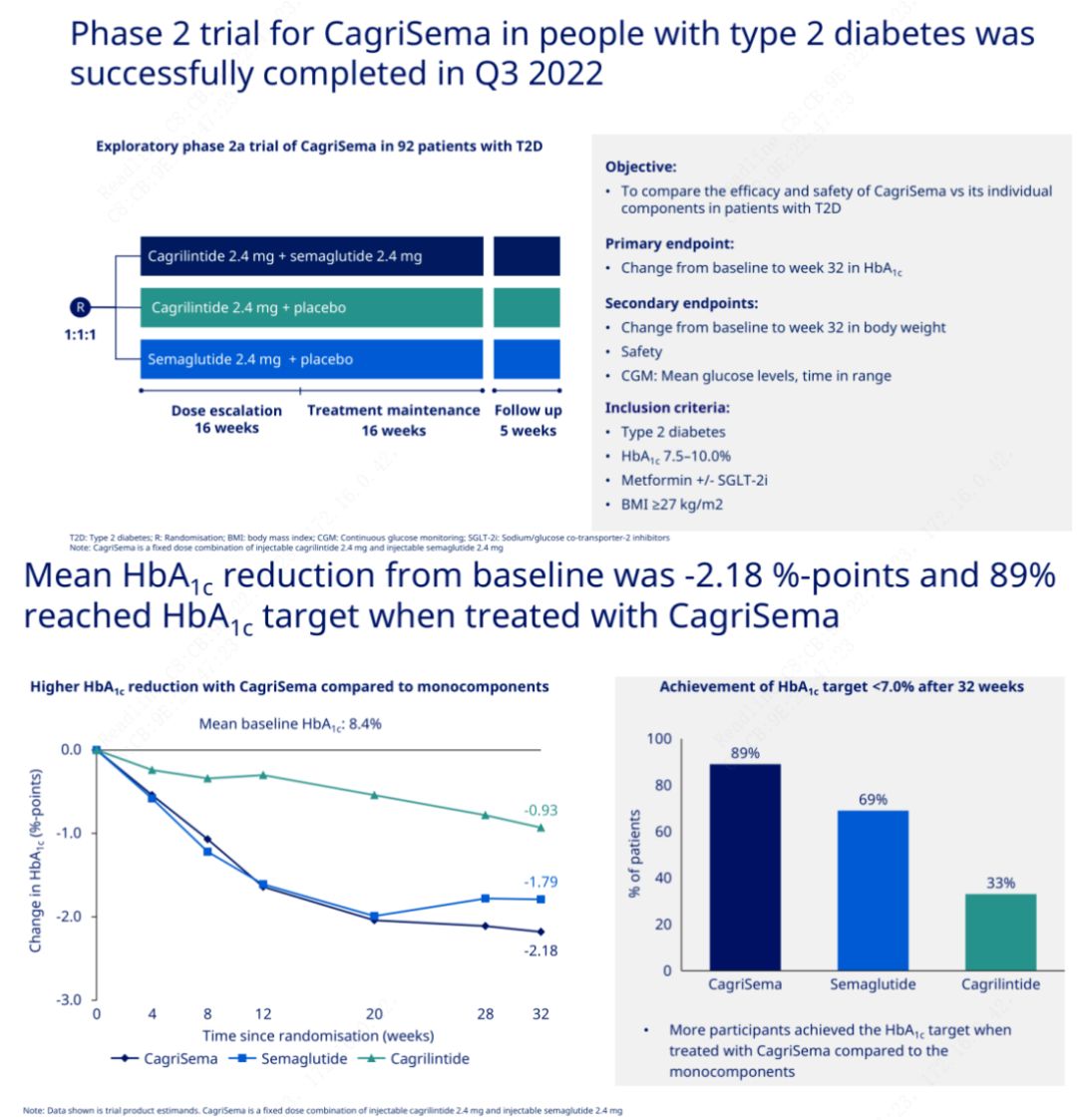
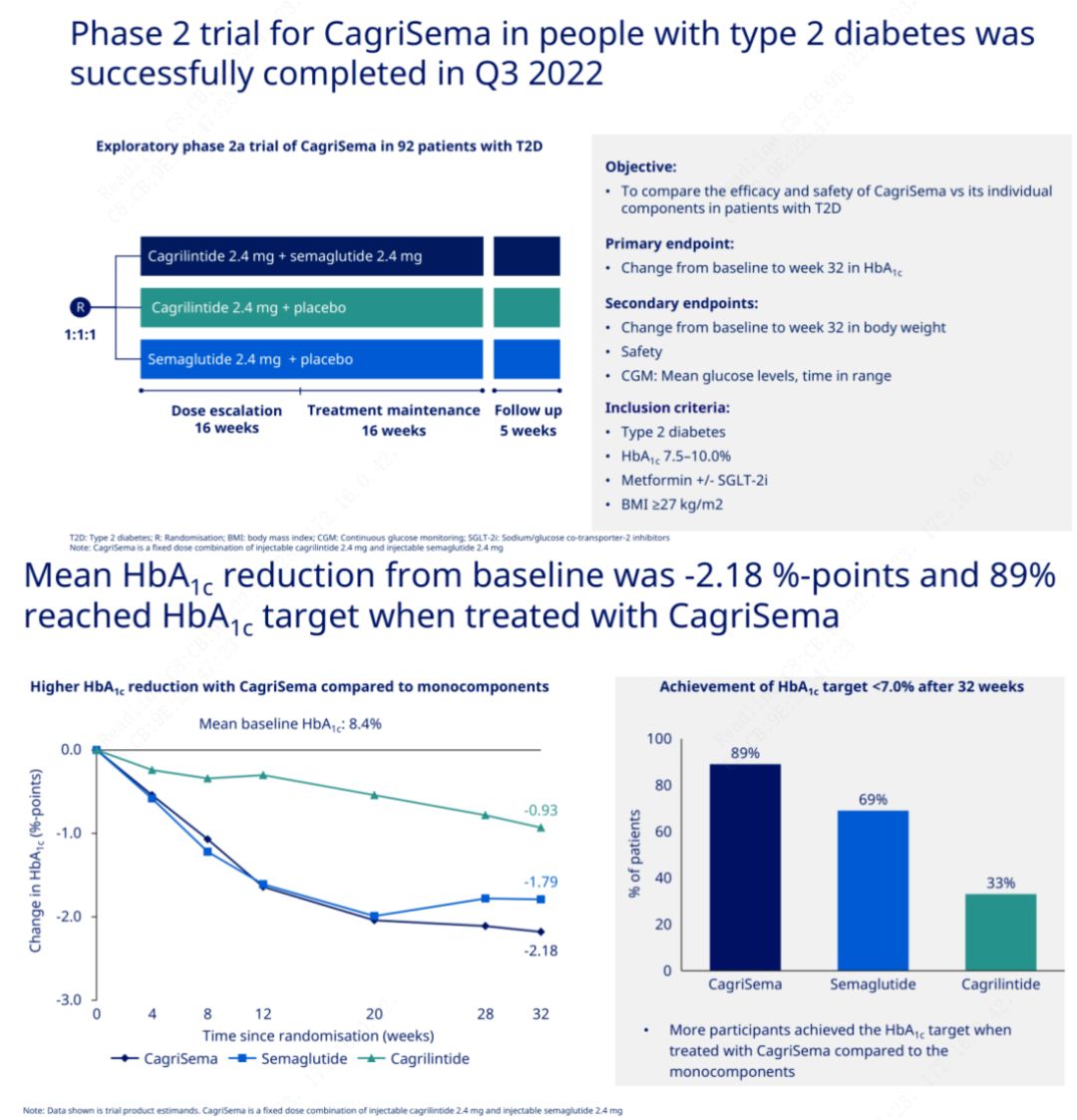
Az adatok azt mutatták, hogy a jelentős hipoglikémiás hatáson túl a CagriSema injekció a fogyás tekintetében szignifikánsan felülmúlta a szemeglutidot (5,1%) és a cagrilintidet (8,1%), 15,6%-os fogyással.
Az innovatív Tirzepatide gyógyszer a világ első jóváhagyott heti GIP/GLP-1 receptor agonistája.Két inkretin hatásait egyesíti egyetlen molekulában, amelyet hetente egyszer injekcióznak, és a 2-es típusú cukorbetegség kezelésének új osztálya.A tirzepatidot az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hatósága (FDA) 2022 májusában hagyta jóvá a 2-es típusú cukorbetegségben szenvedő felnőttek glikémiás kontrolljának (diéta és testmozgás alapján) javítására, és jelenleg az Európai Unióban, Japánban és más országokban engedélyezett.
Július 5-én Eli Lilly bejelentette a III. fázisú SURPASS-CN-MONO tanulmányt a 2-es típusú cukorbetegek kezelésére szolgáló gyógyszer-klinikai vizsgálatok regisztrációs és információközlési platformjáról.A SURPASS-CN-MONO egy randomizált, kettős-vak, placebo-kontrollos III. fázisú vizsgálat, amelynek célja a tirzepatid monoterápia hatékonyságának és biztonságosságának értékelése a placebóval összehasonlítva 2-es típusú cukorbetegségben szenvedőknél.A vizsgálatba 200, 2-es típusú cukorbetegségben szenvedő beteg bevonását tervezték, akik az 1. látogatást megelőző 90 napban semmilyen antidiabetikus gyógyszert nem szedtek (kivéve bizonyos klinikai helyzeteket, mint például akut betegség, kórházi kezelés vagy elektív műtét, rövid távú (≤14). nap) inzulin használata).
A 2-es típusú cukorbetegség engedélyezése várhatóan idén
A múlt hónapban egy SURPASS-AP-Combo tanulmány eredményeit május 25-én tették közzé a Nature Medicine című folyóiratban.Az eredmények azt mutatták, hogy a glargin inzulinnal összehasonlítva a Tirzepatide jobb HbA1c-t és súlycsökkenést mutatott a 2-es típusú cukorbetegek populációjában az ázsiai-csendes-óceáni régióban (főleg Kínában): a HbA1c csökkenése akár 2,49%-kal, a súlycsökkenés pedig akár 7,2 kg-mal (9,4%) a kezelés 40. hetében a vérzsírszint és a vérnyomás jelentős javulása, valamint az általános biztonság és tolerálhatóság jó volt.
A SURPASS-AP-Combo 3. fázisú klinikai vizsgálata a Tirzepatide első vizsgálata, amelyet főként 2-es típusú cukorbetegségben szenvedő kínai betegeken végeztek, Ji Linong professzor, a Pekingi Egyetemi Népi Kórház vezetésével.A SURPASS-AP-Combo összhangban van a globális SURPASS kutatássorozat eredményeivel, amely tovább bizonyítja, hogy a kínai betegek cukorbetegségének patofiziológiája összhangban van a globális betegekével, ami az új gyógyszerek egyidejű kutatásának és fejlesztésének alapja. Kínában és a világban, valamint szilárd bizonyítékokkal alátámasztja, hogy a kínai betegek a lehető leghamarabb alkalmazzák a legújabb cukorbetegség kezelésére szolgáló gyógyszereket és klinikai alkalmazásukat Kínában.
Feladás időpontja: 2023.09.18

